Примерные тестовые задания для подготовки к дифференцированному зачету по химии
1. Органические вещества, в которых углеводородный радикал связан с функциональной гидроксильной группой:
А) алканы, Б) спирты, В) альдегиды, Г) арены.
2.Общая формула алканов:
А) CnH2n Б) CnH2n+2 В) CnH2nOH Г) CnH2n+1OH
3. Выбрать реакцию отщепления воды:
А) CH3-CH2-OH → CH2=CH2 + HOH, Б) CH3-CH2-Br + NaOH → CH2=CH2 + NaBr +HOH,
В) CH2=CH2 + H2 → CH3-CH3, Г) CH2=CH2 + Br2 → Br-CH2-CH2-Br,
4.Связь, возникающая между карбоксильной группой –СООН одной молекулы аминокислоты и аминогруппой NH2 другой аминокислоты в первичной структуре белка:
А) ионная, Б) металлическая, В) пептидная, Г) водородная.
5. Как называется вещество с формулой CH2=CH=СН2:
А) пропан, Б) пропен, В) пропин, Г) пропадиен.
6. Углеводороды, в молекулах которых содержится одна двойная С=С связь:
А) карбоновые кислоты, Б) алкены, В) алкины, Г) алкадиены.
7. Общая формула карбоновых кислот:
А) R-COOH, Б) CnH2n+2 О В) C2(HOH)2 Г) R-COO-R
8. Выбрать реакцию гидрогалогенирования:
А) CH2=CH2 + HOH → CH3-CH2-OH, Б) CH2=CH2 + HBr → CH3-CH2-Br,
В) CH2=CH2 + H2 → CH3-CH3, Г) CH2=CH2 + Br2 → Br-CH2-CH2-Br,
9. Последовательность остатков аминокислот в полимерной цепи белковой молекулы:
А) первичная структура, Б) вторичная структура,
В) третичная структура, Г) четвертичная структура
10. Как называется вещество с формулой CH3-CH2-СООН:
А) пропанол, Б) пропаналь, В) пропановая кислота, Г) пропанон
11. Написать уравнения реакций по схеме: CH4 → СН2=СН2 → С2Н5ОН → С2Н5ОNa.
12. Температурный коэффициент некоторой химической реакции равен 4. Как изменится скорость этой химической реакции при нагревании реакционной смеси от 20 до 50 градусов?
А) увеличится в 80 раз Б) увеличится в 10 раз
В) увеличится в 64 раза Г) уменьшится в 80 раз
13. Какое уравнение соответствует реакции замещения:
А) CO2+H2О → H2CO3, Б) C+2H2 → CH4,
В) 2H2O → 2H2+O2, Г) 2 H2O+2Na → 2NaOH+H2
14.Способность атома химического элемента соединяться с определенным количеством атомов другого элемента:
А) электроотрицательность, Б) радиус, В) валентность, Г) растворимость.
15. В раствор, содержащий 112 г сульфата меди поместили избыток железа. Вычислите, сколько граммов меди может выделиться в этой реакции.
А) 90 Б) 45 В) 62 Г) 77
16. Заряд ядра атома хлора равен: А) +7, Б) +3, В) +17, Г) +35.
17. Наиболее ярко выраженные неметаллические свойства проявляет:
А) бром, Б) фтор; В) хлор, Г) астат.
18. Высший оксид элемента алюминия:
А) Al2O3 Б) AlO В) Al2O5 Г) AlО3.
19. Элементы побочных подгрупп 1-8 групп относятся к элементам:
А) s-семейства, Б) р-семейства, В) d-семейства, Г) f-семейства
20. Какой тип химической связи характерен для вещества с формулой Н2 SO4 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
21. Выберите группу, включающую только кислоты:
А) НBr , BaO, Са(OH)2 Б) SO2 H2S, H2O B) H2O, PH3, SO3 Г) HI, H3PO4, HClO
22. Крахмал среди других веществ можно распознать с реакцией с:
А) с оксидом меди (II), Б) с гидроксидом меди,
В) с оксидом серебра, Г) иодной водой.
23. Названия альдегидов заканчиваются на :
А) –ен, Б) –ол, В) -аль, Г) –ин.
24. Гидролиз вещества NiCl2 происходит:
А) по катиону, Б) по аниону, В) и по катиону, и по аниону, Г) гидролиз не идет.
25. Выберите моносахарид:
А) (С6Н10О5)n Б) С6Н12 О6 В) С12Н22О11 Г) С10Н22
26. Какие продукты реакции образуются при взаимодействии хлора с холодным раствором гидроксида натрия?
А) = NaCl + NaCIO + Н2О Б) = NaCl + Н2О
В) = NaОН + NaCI + Н2О Г) = NaCl(ОН)
27. Как распознать растворимые соли ЖЕЛЕЗА (II) среди других веществ?
А) добавлением натрия, выделяется газ бурый,
Б) при добавлении щелочи выпадает темно-зеленый осадок, буреющий на воздухе,
В) при добавлении лакмуса малиновый цвет,
Г) разлагаются при нагревании с образованием газа с запахом тухлых яиц
28. Органические вещества, молекулы которых состоят только из атомов углерода и водорода:
А) спирт, Б) кислота, В) углевод, Г) углеводород.
29. Общая формула соли:
А) МеnОm, Б) Ме(ОН)n В) HnX Г) МеnХ , где Х – кислотный остаток
30. Выберите уравнение реакции изомеризации:
А) СН2=СН2 + «О» + Н2О → ОН-СН2-СН2-ОН
Б) СН2=СН2 + О2 → Н2О + СО2
В) СН≡СН + Н2О → СН3-СНО
Г) СН2=СН-СН2-СН3 → СН3-СН=СН-СН3
31. Скрученная в спираль полипептидная цепь аминокислот в белке:
А) первичная структура, Б) вторичная структура,
В) третичная структура, Г) четвертичная структура
32. Как называется вещество с формулой CH3- CH2-СНО:
А) пропанол, Б) пропаналь, В) пропановая кислота, Г) пропанон
33. Написать уравнения реакций по схеме: CH4 → C2H2 → C2H3Cl → C2H4 Cl2
1. Углеводороды, в молекулах которых содержится бензольное кольцо:
А) алканы, Б) ароматические, В) алкины, Г) простые.
34. Общая формула углеводов:
А) R-COOH, Б) Cn (H2O)m В) CnHnOH Г) R-COO-R 2
35. Выбрать реакцию отщепления галогеноводорода:
А) CH3-CH2-OH → CH2=CH2 + HOH,
Б) CH3-CH2-Br + NaOH →CH2=CH2 + NaBr +HOH,
В) CH2=CH2 + H2 → CH3-CH3,
Г) CH2=CH2 + Br2 → Br-CH2-CH2-Br,
36. Высокотемпературный нагрев органического вещества или угля без доступа воздуха:
А)крекинг, Б) риформинг, В) перегонка, Г) коксование.
37. Как называется данное вещество с формулой СН3-С≡С-СН3 ?
А) бутин-2, Б) бутаналь, В) бутадиен-1.3, Г) бутановая кислота.
38. Написать уравнения реакций по схеме:
СН3-СН2-СН3 → СН3-СН=СН2 → (-СН - СН2-)n → СО2
СН3
39. При комнатной температуре с наибольшей скоростью протекает реакция между:
А) Zn (порошок) и HCl (1 % р-р) Б) Zn (порошок) и HCl (30 % р-р)
В) Zn (порошок) и HCl (10 % р-р) Г) Zn (гранулы) и HCl (30 % р-р)
40. Окислительно-восстановительной не является реакция:
А) 2Na + Cl2 → 2NaCl Б) 2NaCl + H2 SO4 → Na2 SO4 + 2HCl↑
В) Zn +2HCl → Zn Cl2 + H2 ↑ Г) H2C=O + 2Ag2O → 4 Ag + CO2↑+ H2O
41. Атом, присоединяющий «чужие» электроны в химической реакции:
А) окислитель, Б) восстановитель, В) комплексообразователь, Г) ингибитор.
42. В воде массой 250 г растворили 50 г КОН. Вычислите массовую долю гидроксида калия в растворе в %. А) 20% Б) 16,7% В) 25% Г) 12,6%
43. Какой объем водорода получится при пиролизе 67,2 л метана?
А) 22,4 л, Б) 134,4 л, В) 50,1 л, Г) 8 л.
44. Наиболее ярко выраженные неметаллические свойства проявляет:
А) сера, Б) селен; В) теллур, Г) кислород.
45. Высший оксид элемента лития:
А) Li2O Б) Li2O2 В) Li2O5 Г) LiО3
46. Выберите ряд, включающий только основные оксиды:
А) СuO , BaO, СаO, Б) SO2 N2O5 H2O B) H2O, PH3, SO3 Г) CO, ZnO, ClO
47. Какова степень окисления атома азота в веществе с формулой НNO2 ?
А) +2 Б) + 7, B) + 4 Г) +6 Д) +3 Е) - 3.
48. Какой тип химической связи характерен для вещества с формулой С2Н5ОН?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
49. Какой реакцией можно распознать алкены?
А) обесцвечиванием р-ра KMnO4 Б) выделением бурого газа при нагревании,
В) реакцией с оксидом меди Г) реакцией «серебряного зеркала»
50. Названия карбоновых кислот заканчиваются на:
А) -кислота, Б) –овая кислота, В) -та, Г) –ин.
51. В какую сторону сместится химическое равновесие при увеличении давления
Н2 + I2 --- 2HI +Q ? (если все вещества газы):
А) в сторону продуктов, Б) в сторону реагентов, В) равновесие не сместится .
52. Выберите уравнение реакции расщепления сахарозы:
А) С12Н22О11 + Н2О → С6 Н12О6 + С6 Н12О6
Б) С6 Н12О6 + С6 Н12О6 → С12Н22О11 + Н2О
В) 2С12Н22О11 + 2Н2SО4 → 23С + СО2 + 2SО2 + 24Н2О
Г) 8KClO3 + C12H22O11 → 8КCl + 12CO2 + 11H2O
53. Какие продукты реакции образуются при взаимодействии хлора с водой?
А) = СlО + Н2 Б) = НCl + О2
В) = НСl + HCIО Г) = Cl(ОН)
54. В пронумерованных пробирках даны растворы 2-х солей – хлорида цинка и хлорида натрия. Как распознать раствор хлорид цинка?
А) добавлением серной кислоты, Б) кипячением,
В) добавлением раствора щелочи, Г) нагреванием с медью
55. Органические вещества, в которых углеводородный радикал связан с функциональной гидроксильной группой:
А) алканы, Б) спирты, В) альдегиды, Г) арены.
56.Общая формула алканов:
А) CnH2n Б) CnH2n+2 В) CnH2nOH Г) CnH2n+1OH
57. Выбрать реакцию отщепления воды:
А) CH3-CH2-OH → CH2=CH2 + HOH, Б) CH3-CH2-Br + NaOH → CH2=CH2 + NaBr +HOH,
В) CH2=CH2 + H2 → CH3-CH3, Г) CH2=CH2 + Br2 → Br-CH2-CH2-Br,
58.Связь, возникающая между карбоксильной группой –СООН одной молекулы аминокислоты и аминогруппой NH2 другой аминокислоты в первичной структуре белка:
А) ионная, Б) металлическая, В) пептидная, Г) водородная.
59. Как называется вещество с формулой CH2=CH=СН2:
А) пропан, Б) пропен, В) пропин, Г) пропадиен.
60. Написать уравнения реакций по схеме
CH3COOH → CH2 (Cl)COOH → CH2 (OH)COOH → CH2 (OH)COOK
61. Какой объем кислорода и углекислого газа содержится в 500 м3 воздуха? (Объемная доля кислорода в воздухе – 21%, углекислого газа – 0,04%)
А) 105; 0,20, Б) 10,5; 2, В) 200; 40, Г) 150; 30.
62. Величина, равная отношению массы вещества к массе раствора, выраженная в % называется:
А) масса, Б) массовая доля, В) концентрация, Г) количество вещества.
63. Химическая связь, возникающая между катионами металлов и анионами неметаллов за счет их электростатического притяжения:
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
64. Вычислите объем водорода, который образуется при растворении алюминия массой 8,1 г в воде.
А) 3,6 Б) 6,7 В) 5 Г) 10
65. Количество электронов в атоме брома равно: А) 40, Б) 35, В) 80, Г) 45.
66. Наиболее ярко выраженные металлические свойства проявляет:
А) бор, Б) углерод; В) бериллий, Г) литий.
67. Высший оксид элемента кальция: А) Са2O Б) Са2O2 В) Са2O5 Г) СаО
68. Выберите ряд, включающий только оксиды:
А) СuO , BaO, Са(OН)2, Б) SO2 , HNO3, Cl2O, B) H2O, PH3, SO3 Г) CO, ZnO, ClO
69. Частица Ва2+ называется :
А) электрон бария Б) атом бария В) катион бария Г) анион бария.
70. Железо относится к семейству элементов:
А) s-элементам Б) p-элементам, В) d-элементам Г) f-элементам.
71. Какова массовая доля кислоты в растворе, полученном при смешении 10 г серной кислоты и 50 г воды? Ответ округли до целого числа. А) 10% Б) 20 % В) 15% Г) 17%
72. Расставьте коэффициенты в уравнениях: Аl+ Н2SO4 → Al2(SO4)3 + H2 ;
Чему равен коэффициент перед восстановителем в этом уравнении?
А) 2, Б) 3, В) 4 Г) 6
73. Растительные жиры жидкие, потому что содержат:
А) остатки непредельных кислот, Б) глицерин, В) атомы натрия,
Г) растительные масла тают из-за высокой температуры.
74. Вещества, имеющие очень хорошую теплопроводность и электропроводность, обладающие металлическим блеском, ковкостью и пластичностью:
А) газы Б) металлы, В) неметаллы, Г) кислоты
75. Общая формула оксидов:
А) ЭnОm, Б) Э(ОН)n В) HnX Г) ЭnХ , где Х – кислотный остаток
76. Выберите уравнение реакции окисления:
А) СН2=СН2 + «О» + Н2О → ОН-СН2-СН2-ОН Б) СН2=СН2 + О2 → Н2О + СО2
В) СН=СН + Н2О → СН3-СНО Г) СН2=СН-СН2-СН3 → СН3-СН=СН-СН3
77. Углеводы, не подвергающиеся гидролизу с образованием более простых соединений
А) моносахариды, Б) полисахариды, В) дисахариды, Г) крахмал.
78. Как называется вещество с формулой CH3 –CH2 -СН3:
А) пропан, Б) пропен, В) пропин, Г) пропадиен.
79. Написать уравнения реакций по схеме C2H6 → C2H5Cl → C2H5OH → C2H5O-C2H5
80. Какой металл реагирует с серной кислотой быстрее других?
| А) | Zn Б) Mg, B) Fe, Г) Pb. |
81. Экзотермической является реакция:
А) МgCO3 → MgO + CO2; Б) 2 H2O2 → O2 + 2Н2О
В) S+O2 → SO2; Г) 2 H2O → O2 + 2Н2
82. Процесс отдачи атомом электронов другому виду атома в ходе химической реакции:
А) разложение, Б) ингибирование, В) восстановление, Г) окисление.
83. Технический цинк массой 0.33 г обработали раствором серной кислоты. При этом выделился газ 0.112 л. Вычислить массовую долю цинка в данном образце.
А) 100% Б) 98% В) 90% Г) 87%
84. Количество протонов в атоме гелия равно: А) 2, Б) 14, В) 4, Г) 8.
85. Вещества, в молекулах которых группа –СНО связана с углеводородным радикалом или атомом водорода: А) спирты, Б) альдегиды, В) кислоты, Г) амины.
86. Общая формула алкадиенов:
А) CnH2n Б) CnH2n-2 В) CnH2nOH Г) CnH2n+1OH
87. Выбрать реакцию отщепления галогена:
А) CH3-CH3 → CH2=CH2 + H2, Б) CH3-CH2-Br + NaOH → CH2=CH2 + NaBr +HOH,
В) CH2=CH2 + H2 → CH3-CH3, Г) Br-CH2-CH2-Br + 2К → CH2=CH2 + 2КBr,
88. Разделение жидкой смеси на отдельные компоненты на основании различия их температур кипения: А) газойль, Б) перегонка, В) риформинг, Г) коксование.
89. Как называется данное вещество с формулой СН2 = С=СН-СН3 ?
А) бутин-2, Б) бутаналь-3, В) бутадиен-1,2, Г) бутановая кислота.
90. Написать уравнения реакций по схеме:
СН3-СН3 → СН2= СН2 → СН3-СН2ОН → СН3-СНО
91. Реакция, скорость которой зависит от площади поверхности соприкосновения реагирующих веществ, - это:
а) нейтрализация серной кислоты раствором гидроксида натрия
б) горение водорода в кислороде
в) взаимодействие растворов хлорида меди и гидроксида калия
г) горение алюминия в кислороде
92. К реакциям, идущим без изменения степени окисления, относится реакция между:
А) натрием и хлором; Б) цинком и серой; В) железом и соляной кислотой; Г) раствором хлорида бария и раствором нитрата серебра.
93. Процесс присоединения атомом электронов другого вида атома в ходе химической реакции:
А) разложение, Б) ингибирование, В) восстановление, Г) окисление.
94. При растворении меди в концентрированной серной кислоте выделился оксид серы (IV) объемом 2,8 л. Какая масса меди была взята для реакции?
А) 8 Б) 12 В) 6 Г) 10
95. Количество внешних электронов в атоме фосфора равно: А) 3, Б) 4, В) 5, Г) 6.
96.Органические вещества, молекулы которых содержат карбоксильную группу, связанную с углеводородным радикалом или атомом водорода:
А) спирты, Б) фенолы, В) карбоновые кислоты, Г) анилин.
97. Общая формула алкинов:
А) CnH2n Б) CnH2n-2 В) CnH2nOH Г) CnH2n+1OH
98. Выбрать реакцию замещения: CH3
А) CH3-CH3 +Cl2 → CH3-CH2Cl + HCl, Б) CH3-CH2-CH2-CH3 → CH3-CH-CH3
В) CH2=CH2 + H2 → CH3-CH3, Г) Br-CH2-CH2-Br → CH2=CH2 + Br2,
99. Сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот:
А) белки, Б) жиры, В) углеводы, Г) мыла.
100. К какому классу относится вещество с формулой CH3- CH2-СН2-СН2-ОН:
А) спирт, Б) альдегид, В) карбоновая кислота, Г) амин.
101. Написать уравнения реакций по схеме: C3H8 → C3H6 → C3H7OH → C3H7ONa
102. На какие вещества расщепляется сахароза в организме?
А) глюкоза, Б) глюкоза и фруктоза, В) глюкоза и сахароза, Г) лактоза и глюкоза
103. Состояние обратимого химического процесса, при котором скорости прямой и обратной реакции равны, называется:
А) гомогенность, Б) химическое равновесие, В) катализ, Г) противоток.
104. Химическая связь, возникающая в металлах и сплавах между атом-ионами металлов, осуществляемая совокупностью валентных электронов в кристаллической решетке:
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
105. В 100 мл воды растворили 60 г хлорида натрия. Рассчитать массовую долю соли в растворе в %.
А) 37.5, Б) 70, В) 41,7, Г)100
106. Количество внешних электронов в атоме брома равно: А) 7, Б) 4, В) 5, Г) 6.
107. Наиболее ярко выраженные металлические свойства проявляет:
А) литий, Б) натрий; В) калий, Г) рубидий.
108. Высший оксид элемента алюминия: А) Al2O Б) Al2O2 В) Al2O3 Г) Al2O5
109. Какова степень окисления атома селена в веществе с формулой BaSе?
А) +2 Б) -2 B) + 4 Г) +6 Д) +3 Е) - 3.
110. Восстановление металла из его оксида с помощью более активного металла:
А) металлотермия Б) гидротермия, В) электролиз Г) гидролиз.
111. Какой тип химической связи характерен для вещества с формулой СН4 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
112. От употребления нескольких миллилитров какого спирта человек слепнет или умирает?
А) метилового, Б) этилового, В) пропилового Г) бутилового
113. Какова масса чистого этилового спирта может прореагировать с 23 гр натрия?
А) 23 г, Б) 92 г, В) 230 г, Г) 46 г
114. Названия ароматических углеводородов заканчиваются на: А) -бензол, Б) –ол, В) –аль, Г) -ин
115. Какой реакцией можно распознать простейшие амины?
А) под действием раствора хлоридом железа (III) появляется фиолетовая окраска раствора,
Б) при взаимодействии с активными металлами выделяется газ,
В) обесцвечиванием бромной воды,
Г) изменением цвета лакмуса на синий.
116. Простые вещества с различными физическими свойствами, которые при обычных условиях являются как газами, так и жидкостями или твердыми веществами:
А) металлы, Б) неметаллы, В) оксиды, Г) основания.
117. Общая формула водородных соединений неметаллов:
А) ЭnОm, Б) Э(ОН)n В) HnЭ-n Г) ЭnХ , где Х – кислотный остаток
118. Выберите уравнение реакции гидратации:
А) СН2=СН2 + «О» + Н2О → ОН-СН2-СН2- ОН Б) СН2=СН2 + О2 → Н2О + СО2
В) СН ≡СН + Н2О → СН3-СНО Г) СН2=СН-СН2-СН3 → СН3-СН=СН-СН3
119. Натриевые или калиевые соли высших карбоновых кислот:
А) белки, Б) жиры, В) углеводы, Г) мыла
120. К какому классу относится вещество с формулой CH3-CH2-СН2-СООН:
А) спирт, Б) альдегид, В) карбоновая кислота, Г) амин.
121. Написать уравнения реакций по схеме: C3H6 → C3H7Cl → C3H7OH → C3H7OK
122. Скорость гетерогенной химической реакции измеряется в:
А) с*моль/кг Б) моль/см2 *с; В) м*моль2/с; Г) с *моль/м3
123. Укажите реагенты, взаимодействие которых приводит к следующему сокращенному ионному уравнению реакции: 2H+ + CO32- = H2O + CO2
А) CaCO3 + HCl → Б) CH3COOH→
В) NaHCO3 + HCl→ Г) Na2CO3 + HCl →
124. Разделение нефти на группы продуктов (бензин, керосин и др.) :
А) риформинг, Б) перегонка, В) пиролиз, Г) крекинг.
125. При взаимодействии хлора с иодидом калия был получен йод массой 50,8 г. Определите объем хлора, который необходим для данной реакции.
А) 4,48 л Б) 22,4 л В) 5,08 м3 Г) 12,9 м3
126. Органические вещества, в которых углеводородный радикал соединен с аминогруппой:
А) анилины, Б) амины, В) алканы, Г) алкины.
127. Общая формула оксидов:
А) Ме+n(OH)n Б) Hn(кисл ост), В) Ме (кисл ост), Г) ЭO
128. Выбрать реакцию присоединения : CH3
А) CH3-CH3 +Cl2 → CH3-CH2Cl + HCl, Б) CH3-CH2-CH2- CH3 → CH3-CH- CH3
В) CH2=CH2 + H2 → CH3-CH3, Г) Br-CH2-CH2-Br → CH2=CH2 + Br2,
129. Какой из продуктов коксования каменного угля используется в металлургии?
А) коксовый газ, Б) каменноугольная смола, В) кокс, Г) надсмольная вода.
130. Как называется данное вещество с формулой НО-СН2-СН2-СН2-СН3?
А) бутин-2, Б) бутаналь-3, В) бутанол-1, Г) бутановая кислота.
131. Написать уравнения реакций по схеме: СН4 → СН3Cl → СН3-ОН → НСНО
132. Равновесие в системе 3О2 (г) → 2О3(г) – Q сместится вправо при уменьшении:
А) температуры Б) концентрации кислорода
В) давления Г) концентрации озона
133. Установите причину необратимости реакции: 2NaOH + CuSO4 → Cu(OH)2 + Na2SO4
А) выделение газа Б) образование воды
В) образование осадка Г) реакция не идет до конца.
134. Обменное взаимодействие веществ с водой, приводящее к их разложению:
А) гидролиз, Б) электролиз, В) гексолиз, Г) прополис.
135. Какой объем углекислого газа образуется при сжигании 67,2 л ацетилена С2Н2 ?
А) 67,2 л Б) 98,4 л В) 155,1 л Г) 134,4 л
136. Количество электронных слоев в атоме фосфора равно: А) 3, Б) 2, В) 1, Г) 4.
137. Наиболее ярко выраженные металлические свойства проявляет:
А) кислород, Б) фтор; В) берилий, Г) литий.
138. Высший оксид элемента углерода: А) СO Б) СO2 В) СO3 Г) СO4
139. Какой тип химической связи характерен для вещества с формулой Р4 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
140. Раствор, содержащий очень малое количество растворенного гидроксида натрия, называется:
А) насыщенный Б) разбавленный B) концентрированный Г) ненасыщенный
141. Органические вещества, в молекулах которых содержатся одновременно и карбоксильная, и аминогруппа: А) простые эфиры, Б) анилин, В) аминокислоты, Г) сложные эфиры.
142. Общая формула оснований:
А) Ме+n(OH)n Б) Hn(кисл ост), В)Ме (кисл ост), Г) ЭO
143. Выбрать реакцию изомеризации :
А) CH3-CH3 +Cl2 → CH3-CH2Cl + HCl, Б) CH3-CH2-CH2- CH3 → CH3-CH- CH3
CH3
В) CH2=CH2 + H2 → CH3-CH3, Г) Br-CH2-CH2-Br → CH2=CH2 + Br2,
144. Водный 10%-ный раствор метаналя называется:
А) формалин, Б) карболка, В) жир, Г) глюкоза.
145. К какому классу относится вещество с формулой CH3- CH2-СН2- СН2- CHO:
A) спирт, Б) альдегид, В) карбоновая кислота, Г) амин.
146. Написать уравнения реакций по схеме: C4H8 → C4H8Cl2 -→ C4H8 → C4H6
147. Вещество, увеличивающее скорость реакции:
А) катализаторы, Б) энзимы, В) ингибиторы, Г) окислители
148. Величина, равная отношению объема данного газа к общему объему газовой смеси, выраженная в %, называется:
А) объемная масса, Б) объемная доля, В) концентрация, Г) количество вещества.
149. Химическая связь, возникающая между атомом водорода одной молекулы и электроотрицательным атомом другой молекулы, называется:
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
150. Вычислите скорость реакции при увеличении температуры от 10 градусов до 60 градусов, если начальная скорость реакции равна 0,2 моль/л*сек, а температурный коэффициент равен 2.
А) 0.4, Б) 3.7 В) 6.4 Г) 8.5
151. Количество электронных слоев в атоме меди равно: А) 3, Б) 6, В) 5, Г) 4.
152. Наиболее ярко выраженные металлические свойства проявляет:
А) хлор, Б) сера; В) алюминий, Г) магний.
153. Высший оксид элемента фосфора: А) РO Б) РO2 В) Р2O3 Г) Р2О5.
154. Какой тип химической связи характерен для вещества с формулой Сu?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
155. Какова степень окисления атома кремния в веществе с формулой Li4Si?
А) +2 Б) -2 B) + 4 Г) -4 Д) -3 Е) - 1.
156.Органические вещества – природные полимеры, образованные остатками аминокислот:
А) крахмал, Б) анилин, В) аминокислоты, Г) белки.
157. Общая формула кислот: А) Ме+n(OH)n Б) Hn(кисл ост), В)Ме (кисл ост), Г) ЭO
158. Выбрать реакцию полимеризации : Kat
А) CH3-CH3 +O2 → CO2 + H2O, Б) CH3-CH3 +O2 → CH3-COOH + HOH
В) nCH2=CH2 → (-CH2-CH2-)n, Г) CH3-COOH + C2 H5-OH → CH3-COO-C2 H5 +HOH
159. Этиленгликоль применяют в качестве … :
А) окислителя, Б) антифриза, В) катализатора, Г) каучука.
160. Как называется вещество с формулой: ![]()
А) бензол, Б) фенол, В) толуол. Г) анилин.
161. Написать уравнения реакций по схеме: C6H14 → C6H12 → C6H6 → C6H5NO2
162. Температурный коэффициент реакции равен 2,5. Как изменится ее скорость при охлаждении реакционной смеси от изменения температуры от 50 °С до 30 °С?
А) уменьшится в 6,25 раз, Б) увеличится в 20 раз,
В) уменьшится в 5 раз, Г) увеличится в 25 раз
163. Укажите реакцию разложения.
А) CaO+H2O → Ca(OH)2; Б) S+O2 → SO2;
В) 2CO+O2→ 2CO2; Г) MgCO3→ MgO+CO2.
164. Какой способ получения металла включает следующие 2 этапа: обжиг и восстановление металла? А) электрометаллургия, Б) гидрометаллургия,
В) пирометаллургия, Г) металлургия.
165. Определите коэффициент перед окислителем: С4 Н6 + O2 = СО2 + Н2О
А) 3, Б) 7, В) 11, Г) 17, Д) 6, Е) 20
166. Атомная масса атома аргона равна: А) 18, Б) 39, В) 3, Г) 40.
167. Наиболее ярко выраженные металлические свойства проявляет:
А) мышьяк, Б) цинк; В) медь, Г) калий.
168. Неорганические вещества, которые при растворении в воде образуют катионы водорода:
А) кислоты, Б) основания, В) спирты, Г) альдегиды.
169. Общая формула оснований:
А) ЭnОm, Б) Э(ОН)n В) HnЭ-n Г) ЭnХ , где Х – кислотный остаток
170. Выберите уравнение реакции полимеризации:
А) nСН2=СН2 → (-СН2-СН2-)n Б) СН2=СН2 + О2 → Н2О + СО2
В) СН=СН + Н2О → СН3-СНО Г) СН2=СН- СН2- СН3 → СН3- СН= СН- СН3
171. Вещества, имеющие одинаковый состав, но разное строение:
А) гомологи, Б) радикалы, В) изомеры, Г) гидраты.
172. Как называется вещество с формулой: ![]()
А) бензол, Б) фенол, В) толуол. Г) анилин
173. Написать уравнения реакций по схеме: CH4 → C2H2 → C2H2Cl2 → C2H2 (OH) 2
174. Определите коэффициент перед кислородом: СН3NH2 + O2 → CO2 + H2O + N2
А) 3, Б) 6, В) 9, Г) 12
175. Укажите гетерогенную реакцию.
А) 2CO+O2=2CO2; Б) H2+Cl2=2HCl;
В) 2SO2+O2=2SO2 (кат V2O5); Г) Nа2O+H2О=NаOН.
176. Какой способ получения металла включает следующие 2 этапа: 1)растворение в кислоте нерастворимой в воде руды и 2) восстановление металла:
А) электрометаллургия, Б) гидрометаллургия,
В) пирометаллургия, Г) металлургия.
177. Вычислите, во сколько раз увеличится скорость реакции при повышении температуры от 30 до 70 градусов С, если температурный коэффициент скорости равен 2.
А) 24 Б) 16 В) 8 Г) 48
178. Общее количество электронов в атоме кремния равно: А) 14, Б) 28, В) 32, Г) 16.
179. Наиболее ярко выраженные неметаллические свойства проявляет:
А) натрий, Б) кремний, В) хлор, Г) алюминий.
180. Высший оксид элемента серы: А) SO Б) SO2 В) SO3 Г) SO4
181. Какой тип химической связи характерен для вещества с формулой СaC2 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
182. Какова степень окисления атома азота в веществе с формулой HNO2 ?
А) +2 Б) -2 B) + 4 Г) +6 Д) +3 Е) - 3.
183. Как определить главную подгруппу элементов в периодической системе?
А) в ней больше элементов, Б) по самому верхнему элементу,
В) по цвету «клеток» , Г) по номеру группы.
184. Почему в жесткой воде мыло не стирает?
А) некоторые сорта мыла хорошо стирают в жесткой воде,
Б) вещества мыла реагируют с солями воды и образуют осадок,
В) ионы натрия и калия создают щелочную реакцию раствора,
Г) мыло подвергается гидролизу.
185. Сплав массой 50 г содержит 20% алюминия и 80% магния. Вычислите массу магния в этом сплаве.
А) 80 г, Б) 40 г, В) 10 г, Г) 20 г.
186.Углеводороды, в молекулах которых содержатся двойные или тройные связи:
А) предельные, Б) непредельные, В) спиртовые, Г) сложные.
187. Общая формула сложных эфиров:
А) R-CnH2n Б) R-CОО-R В) R-CHO Г) CnH2n+1OH
188. Выбрать реакцию мягкого окисления : Kat
А) CH3-CH3 +O2 → CO2 + H2O, Б) CH3-CH3 +O2 → CH3-COOH + HOH
В) nCH2=CH2 → (-CH2-CH2-)n, Г) CH3-COOH + C2 H5-OH → CH3-COO-C2 H5 +HOH
189. Остаток после перегонки мазута, который используется для получения битума и асфальта (применяется в дорожном строительстве):
А) гудрон Б)газойль В) керосин, Г) лигроин
190. Как называется данное вещество с формулой СН3-СН2- СН2- СООН?
А) бутин-2, Б) бутаналь-3, В) бутанол-1, Г) бутановая кислота.
191. Написать уравнения реакций по схеме:
СН3-СНО → СН3-СН2ОН → СН2= СН2 → СН2Br - СН2Br
191. Электролитом не является: А) серная кислота, Б) спирт,
В) гидроксид натрия, Г) раствор оксида углерода(II).
192. Укажите гомогенную реакцию.
а) CaO+H2O → Ca(OH)2; б) S+O2 → SO2; в) 2CO+O2 → 2CO2; г) MgCO3 → MgO+CO2.
193. Разрушение металлов и сплавов под воздействием окружающей среды:
А) окисление, Б) агрегация, В) коррозия, Г) омыление.
194. Реакция протекает по уравнению А+В = 2С. Начальная концентрация вещества А равна 0,22 моль/л, а через 10 с — 0,215 моль/л. Вычислите среднюю скорость реакции.
А) 0, 001 моль/л*с, Б) 0, 05 моль/л*с, В) 0,0005 моль/л * с Г) 5 моль/л*с
195. Количество элементов в 4 периоде Периодической системы Менделеева:
А) 2, Б) 8, В) 18, Г)32.
.
196. Наиболее ярко выраженные неметаллические свойства проявляет:
А) олово, Б) кремний, В) углерод, Г) германий.
197. Высший оксид элемента хлора:
А) Cl2 O3 Б) Cl2 O5 В) Cl2 O7 Г) Cl2 O.
198. Какой тип химической связи характерен для вещества с формулой Li3N ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
199. Частицы 15О, 16О являются:
А) изотопами Б) изобарами, В) изотонами Г) изотермами
200. Очистка металлов от примесей с помощью процесса электролиза называется:
А) рафинирование Б) гальваностегия В) гальванопластика Г) пирометаллургия.
201. Щелочные металлы находятся в Периодической системе:
А) в 4 группе, Б) в 3 группе, В) в 1 группе, Г) в 2 группе
202. Какой реакцией можно распознать карбоновые кислоты среди других веществ?
A) Аммиачного раствора оксида серебра.
B) Бромной воды.
Б) Раствора хлорида железа (III).
Г) Лакмуса.
203. Углеводороды, в молекулах которых все атомы углерода образуют простые (одинарные) связи С-С или С-Н: А) алкены, Б) алканы, В) арены, Г) сложные эфиры.
204.Общая формула спиртов: А) CnH2n Б) CnH2n+2 В) CnH2nOH Г) CnH2n+1OH
205. Выбрать реакцию гидратации:
А) CH2=CH2 + HOH → CH3-CH2-OH, Б) CH2=CH2 + HBr → CH3-CH2-Br,
В) CH2=CH2 + H2 → CH3-CH3, Г) CH2=CH2 + Br2 → Br-CH2-CH2-Br,
206. Переработка нефтепродуктов, при которой происходит разрыв молекул углеводородов на более короткие молекулы:
А) крекинг, Б) риформинг, В) перегонка, Г) коксование.
207. Как называется данное вещество с формулой СН3- СН2-СН2-СНО ?
А) бутин, Б) бутаналь, В) бутадиен-1.3, Г) бутановая кислота.
208. Написать уравнения реакций по схеме: С2Н2 → С6Н6 → С6Н5Вr → С6Н5ОН
209. Полимерные материалы, способные приобретать заданную форму при изготовлении изделия и сохранять ее в процессе эксплуатации:
А) пластмассы, Б) белки, В) каучуки, Г) волокна.
210. Какое уравнение соответствует реакции разложения:
А) Zn+CuSO4 → ZnSO4+Cu Б) BaCl2+K2CO3 → BaCO3+2KCl,
В) CaO+CO2 → CaCO3, Г) Fe(OH)2 → FeO+H2O.
211. Вещества, образованные несколькими химическими элементами:
А) простые, Б) сложные, В) составные, Г) комплексные.
212. Как необходимо изменить температуру в системе, чтобы скорость химической реакции увеличить в 81 раз. Температурный коэффициент равен 3?
А) повысить на 10 градусов Б) повысить на 20 градусов
В) повысить на 30 градусов Г) повысить на 40 градусов
213. Заряд ядра атома углерода равен:
А) +12, Б) +4, В) +2, Г) +6.
214. Наиболее ярко выраженные неметаллические свойства проявляет:
А) бром, Б) селен; В) германий, Г) мышьяк.
215. Высший оксид элемента меди: А) Cu2O Б) Cu2O7 В) Cu2O5 Г) CuО.
216. Выберите ряд, включающий только основные оксиды:
А) СuO , BaO, СаO, Б) SO2 N2O5 H2O
B) H2O, PH3, SO3 Г) CO, ZnO, ClO
217. Углеводороды, в молекулах которых содержится одна тройная С ≡ С связь:
А) карбоновые кислоты, Б) алкены, В) алкины, Г) амины.
218. Общая формула сложных эфиров: А) R-COOH, Б) CnH2n+2 В) CHOH Г) R-COO-R1
219. Выбрать реакцию галогенирования:
А) CH2=CH2 + HOH → CH3-CH2-OH, Б) CH2=CH2 + HBr → CH3-CH2-Br,
В) CH2=CH2 + H2 → CH3-CH3, Г) CH2=CH2 + Br2 → Br-CH2-CH2-Br,
220. Трехмерная структура белковой молекулы в пространстве в виде клубочков и волокон:
А) первичная структура, Б) вторичная структура,
В) третичная структура, Г) четвертичная структура.
221. Как называется вещество с формулой CH3- CH2-СН2-NH2:
А) пропановая кислота, Б) пропилацетат, В) пропиламин, Г) пропанон
222. Написать уравнения реакций по схеме: C2H2 → CH3CHO → CH3COOH → CH3COOK
223. Для увеличения скорости химической реакции Mg(тв) + 2Н+ = Mg+2 + H2(г) + 462 кДж необходимо:
А) уменьшить концентрацию ионов водорода
Б) увеличить концентрацию ионов водорода
В) понизить температуру Г) повысить давление.
224. Гомогенной является реакция:
А) H2 + Cl2 → 2HCl Б) Fe(OH)2 → FeO+ H2 O В) Zn +2HCl→ Zn Cl2 + H2 Г) H2SO4 + Ag2O → Ag2 SO4 + H2O
225. Атом, отдающие свои внешние электроны другому атому в химической реакции:
А) окислитель, Б) восстановитель, В) комплексообразователь, Г) ингибитор
226. Сколько граммов хлорида натрия нужно дл приготовления 1500 г раствора, с массовой долей соли в нем 0,9% ? А) 13.5 Б) 15 В) 9 Г) 12.6
227. Количество нейтронов в атоме брома равно: А) 40, Б) 35, В) 80, Г) 45.
228. Наиболее ярко выраженные металлические свойства проявляет:
А) бор, Б) углерод; В) бериллий, Г) литий.
229. Высший оксид элемента хрома: А) Сr2O Б) Сr2O2 В) Сr2O5 Г) СrО Д) Сr2 О3
230. Выберите ряд, включающий только кислотные оксиды:
А) СuO , BaO, СаO, Б) SO2 N2O5 Cl2O7
B) H2O, PH3, SO3 Г) CO, ZnO, ClO
231. Положительно заряженные ионы:
А) электроны Б) протоны В) катионы Г)анионы.
232. Какой из металлов можно получить только электролизом расплавов различных его солей? А) никель, Б) литий, В) медь, Г) железо
233. Какой химической реакцией можно распознать ацетилен среди других непредельных углеводородов?
А) реакцией с аммиачным раствором оксида серебра,
Б) с помощью бромной воды,
В) с помощью раствора перманганата калия,
Г) реакцией с магнием
234. Рассчитайте массу брома, который может присоединить этилен объемом 224 л.
А)1600 г Б) 1000 г В) 2240 г Г) 560 г
235. Какое из веществ обесцвечивает раствор перманганата калия (марганцовки)?
А) пентан, Б) пропан, В) пропен, Г) бензол
236. Соли постоянной жесткости можно удалить из воды:
А) кипячением, Б) добавлением соды,
В) добавлением кислоты Г) добавлением яичного белка
237. О наличии какого химического элемента говорит окрашивание пламени в сине-зеленый цвет при внесении образца органического вещества с помощью медной проволоки в пламя спиртовки?
А) С, Б) Н, В) О, Г) Сl.
238. Закончить уравнение реакции: Al + H2O =
A) = Al(OH)3 + H2↑ Б) = Al2O3 + H2↑ В) = AlH3 + O2↑ Г) = AlH2 +O
239. Выберите уравнение реакции, происходящее с перекисью водорода при обеззараживании раны?
А) 2Н2О → 2Н2 + О2 Б) 2Н2О2 → 2Н2О + О2
В) 2Н2 + О2 → 2Н2О Г) 2Н2О + О2 → 2Н2О2
240. Органическое вещество, в молекулах которых гидроксильная группа ОН связана с бензольным кольцом: А) фенолы, Б) бензол, В) многоатомные спирты, Г) простые эфиры.
241. Общая формула алкенов: А) CnH2n Б) CnH2n+2 В) CnH2nOH Г) CnH2n+1OH
242. Выбрать реакцию отщепления водорода:
А) CH3-CH3 → CH2=CH2 + H2, Б) CH3-CH2-Br + NaOH →CH2=CH2 + NaBr +HOH,
В) CH2=CH2 + H2 → CH3-CH3, Г) Br-CH2-CH2-Br → CH2=CH2 + Br2,
243. Углеводы, в молекулах которых содержится множество молекул простых сахаров
А) моносахариды, Б) полисахариды, В) дисахариды, Г) крахмал.
244. Как называется вещество с формулой CH ≡ C -СН3:
А) пропан, Б) пропен, В) пропин, Г) пропадиен.
245. Написать уравнения реакций по схеме: CH4 → CH3Cl → CH3OH → CH3OLi
246. Одинаковые кусочки магния взаимодействуют с наибольшей скоростью с соляной кислотой если: А) разбавить кислоту, Б) увеличить концентрацию кислоты,
В) увеличить давление, Г) уменьшить температуру.
247. Укажите тип следующей реакции: nCH2 =CH2 → (-CH2 —CH2-)n
А) реакция галогенирования Б) реакция полимеризации
В) реакция окисления Г) реакция гидрирования
248. Кварцевый песок и сода являются основным сырьем для производства:
А) серной кислоты, Б) цемента, В) стекла, Г) масляных красок.
249. Определить массовую долю воды в кристаллогидрате Na2SO4*10H2O.
А) 180 Б) 74 В) 15 Г) 55,9
250. Количество внешних электронов в атоме алюминия равно: А) 3, Б) 4, В) 5, Г) 6.
251. Наиболее ярко выраженные металлические свойства проявляет:
А) кальций, Б) скандий; В) калий, Г) титан.
252. Высший оксид элемента бора: А) В2O Б) В2O2 В) В2O3 Г) В2O5.
253. Отрицательно заряженный электрод при электролизе называется:
А) катод Б) анод В) катионы Г) анионы.
254. Восстановление металла из его оксида с помощью более активного металла:
А) металлотермия Б) гидротермия, В) электролиз Г) гидролиз.
255. Какой тип химической связи характерен для вещества с формулой СН4 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
256. Какой химической реакцией можно распознать растворимые в воде многоатомные спирты среди других веществ?
А) реакцией с оксидом меди при нагревании,
Б) реакцией с раствором перманганата калия в кислой среде
В) реакцией со свежеприготовленным гидроксидом меди без нагревания,
Г) реакцией со свежеприготовленным гидроксидом меди при нагревании,
257. Какой объем воздуха потребуется для сжигания 100 г сульфида цинка?
А) 165 Б) 270 В) 330 Г) 97
258. Производные карбоновых кислот, в которых атом водорода замещен на углеводородный радикал: А) карбоновые кислоты, Б) простые эфиры, В) спирты, Г) сложные эфиры
259. Общая формула аренов: А) CnH2n+6 Б) CnH2n-6 В) CnH2n Г) CnH2n+1O
260. Выбрать реакцию отщепления: CH3
А) CH3-CH3 +Cl2 → CH3-CH2Cl + HCl, Б) CH3-CH2-CH2- CH3 -→ CH3-CH- CH3
В) CH2=CH2 + H2 →- CH3-CH3, Г) Br-CH2-CH2-Br → CH2=CH2 + Br2,
261. Щелочной гидролиз жира с образованием глицерина и натриевой соли карбоновой кислоты:
А) окисление, Б) омыление, В) расщепление, Г) изомеризация.
262. К какому классу относится вещество с формулой CH3- CH2-СН2- СН2- NH2:
А) спирт, Б) альдегид, В) карбоновая кислота, Г) амин.
263. Написать уравнения реакций по схеме: C4H10 → C4H8 → C4H6 → CO2
264. Определите коэффициент перед кислородом: С6 Н6 + O2 = СО2 + Н2О
А) 3, Б) 7, В) 15, Г) 17
265. Установите тип гидролиза Na2S:
А) по катиону, Б) по аниону, В) по катиону и аниону, Г) гидролиз не идет.
266. Окислительно-восстановительная реакция, проходящая на электродах при пропускании постоянного электрического тока через раствор и расплав электролита:
А) гидролиз, Б) электролиз, В) гексолиз, Г) прополис.
267.Органические вещества, в молекулах которых содержатся одновременно и карбоксильная, и аминогруппа: А) простые эфиры, Б) амины, В) аминокислоты, Г) сложные эфиры.
268. Общая формула cоли:
А) Ме+n(OH)n Б) Hn(Кисл ост), В)Ме (Кисл ост), Г) ЭO
269. Выбрать реакцию горения: Kat
А) CH3-CH3 +O2 → CO2 + H2O, Б) CH3-CH3 +O2 → CH3-COOH + HOH
В) nCH2=CH2 → (-CH2-CH2-)n,
Г) CH3-COOH + C2 H5-OH → CH3-COO-C2 H5 +HOH
270. Вещества, ускоряющие химические реакции:
А) катализаторы, Б) ферменты, В) алкины, Г) оксиды.
271. Как называется вещество с формулой: ![]()
А) бензол, Б) фенол, В) бензол. Г) анилин.
272. Написать уравнения реакций по схеме:
CH3COOH → CH3COOLi → CH3COOH → CH3COO-C3H7
273. Продуктом взаимодействия бутена-1 с бромоводородом является
А) 1-бромбутен-2 Б) 1,2-дибромбутан В) 2-бромбутан Г) 1,2-дибромбутен-2
274. Величина, равная отношению количества вещества на объем раствора, выраженная в %, называется: А) масса, Б) объемная доля, В) концентрация, Г) количество вещества.
275. Вещества, образованные всего одним химическим элементом:
А) простые, Б) сложные, В) составные, Г) комплексные.
277. Сколько граммов нитробензола образуется после нитрования 19,5 г бензола?
А) 12,3 Б) 7,8 В) 30,75 Г) 61,5
278. Число электронов в атоме кислорода равно: А) 8, Б) 16, В) 6, Г) 2.
279. Наиболее ярко выраженные неметаллические свойства проявляет:
А) иод; Б) теллур; В) сурьма, Г) олово.
280. Высший оксид элемента брома: А) Br2O Б) Br2O7 В) Br2O5 Г) BrО3
281. Выберите группу, включающую только алкены:
А) SO2 , BaO, С2Н2 Б) С2Н4, С3Н8, СН4 B) С4Н8, С3Н6, С2Н4 Г) С2Н2, C6Н10, С5Н10
282. Элементы побочных подгрупп 1-8 групп относятся к элементам:
А) s-семейства, Б) р-семейства, В) d-семейства, Г) f-семейства
283. Какой тип химической связи характерен для вещества с формулой С2 Н4 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
284. С каким электродом необходимо соединить железный предмет для покрытия серебром способом электролиза раствора нитрата серебра?
А) анодом, Б) анодом и катодом, В) ни с каким, Г) катодом.
285. Какая масса глюкозы образуется клетками растения, если в реакцию вступает 224 л углекислого газа. А) 200 Б) 400 В) 300 Г) 500
286. Какие связи образуются при взаимодействии аминокислот в ходе образования белка?
А) водородные, Б) дисульфидные, В) гидрофобные, Г) пептидные
287. Диссоциацию кислот и солей на ионы под действием воды объяснил:
А) Менделеев, Б) Бутлеров, В) Аррениус, Г) Зинин.
288. Какую формулу имеет вещество с необычным названием «силан»?
А) SO2, Б) SiH4 В) SrO Г) H2Se
289. Почему алюминиевая посуда не растворяется при приготовлении еды в воде?
А) алюминий пассивный металл, не реагирует с водой
Б) поверхность алюминия покрывается оксидной пленкой
В) в алюминий добавлены специальные примеси
Г) нет, алюминий реагирует с водой, поэтому такая посуда через определенное время разрушается.
290. Какая из реакций не идет?
А) Cu + H2O = CuO + H2↑ Б) 2 Cu +O2 =2CuO
B) Cu + Br2 = CuBr2 Г) 3 Cu + 8HNO3 = 3 Cu(NO3)2 + 2NO + 4H2O
291. Рассчитайте скорость реакции между растворами хлорида калия и нитрата серебра, концентрации которых составляют соответственно 0,2 и 0,3 моль/л, а k=1,5∙10-3 л/моль*с.
А) 300 моль/л*с, Б) 900 моль/л*с, В) 0.009 моль/л*с, Г) 0, 00009 моль/л*с,
292. Атомная масса атома фосфора равно: А) 15, Б) 31, В) 3, Г) 30.
293. Наиболее ярко выраженные металлические свойства проявляет:
А) кальций, Б) калий; В) скандий, Г) титан
294. Высший оксид элемента натрия: А) Na2O Б) Na2O2 В) Na2O5 Г) NaО3
295. Какой тип химической связи характерен для вещества с формулой S8 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
296. Раствор, содержащий очень малое количество растворенного гидроксида натрия, называется:
А) насыщенный Б) разбавленный
B) концентрированный Г) ненасыщенный
297. Применяемые в быту металлические предметы (кастрюли) можно защитить от коррозии с помощью: А) протектора Б) минерального масла В) ингибитора Г) эмали
298. Какой химической реакцией можно распознать наличие пи-связи в олеиновой кислоте?
А) реакцией с оксидом меди при нагревании,
Б) реакцией с раствором перманганата калия,
В) реакцией со свежеприготовленным гидроксидом меди без нагревания,
Г) реакцией со свежеприготовленным гидроксидом меди при нагревании,
299. Сколько граммов воды содержит 500 г раствора хлорида калия с массовой долей соли 5%?
А) 450 Б) 100 В) 570 Г) 475.
300. Какой формулой можно определить массу жидкости, исходя из ее объема? .
А) m = V *M, Б) M = n *Mr В) m = V *p Г) Mr = p / m
301. Названия углеводородов с тройной связью заканчиваются на:
А) –ол, Б) – ан, В) – ен, Г) –ин.
302. С чем связано закономерное усиление кислотных свойств и соответственно ослабление основных свойств водородных соединений элементов одного периода?
А) с увеличением полярности связи Э—Н, Б) с уменьшением полярности связи Э—Н,
В) ни с чем не связано, Г) все зависит от того, с каким веществом происходит реакция.
303. Как можно распознать соединения щелочного металла натрия среди других веществ?
А) при добавлении серы образуется бурая жидкость
Б) по цвету пламени – желтый цвет,
В) при сильном нагревании разлагаются, выделяя газ со специфическим запахом,
Г) никак нельзя распознать.
304. Продолжите уравнение реакции: CaCO3 + H2O + CO2→
А) → Ca(OH)2 + H2CO3 Б) → Ca(HCO3)2 + H2O
В) → СаС2 + Н2СО3 Г) → Ca(HCO3)2
305. Межмолекулярное взаимодействие молекул воды происходит зачет образования:
А) ковалентной связи, Б) ионной связи, В) водородной связи, Г) металлической связи.
306. Что означает понятие «технический карбид кальция»?
А) используется в технике, Б) получают с использованием сложной техники и механизмов
В) является изотопом технеция, Г) содержит примеси.
307. Если неметалл образует два или более кислородсодержащих кислот, то самой сильной является какая из них?
А) все одинаковой силы,
Б) с самой маленькой степенью окисления данного неметалла,
В) с самой большой степенью окисления данного неметалла,
Г) все зависит от того, с каким веществом вступает в реакцию.
308. О каком веществе идет речь в описании: «бесцветная гигроскопичная жидкость, c резким запахом, «дымит» на воздухе, неограниченно растворимая в воде, при хранении на свету разлагается и приобретает желтоватый цвет»?
А) аммиачная селитра, Б) азотная кислота, В) гидроксид бария, Г) этиловый спирт
t
309. Выбрать правую часть уравнения для реакции: Cr + O2 →
A) → CrO, Б) →CrO2 В) →CrO3 Г) →Cr2O3
310. Какова степень окисления атома азота в веществе с формулой НNO3 ?
А) +2 Б) + 5, B) + 4 Г) +6 Д) +3 Е) - 3.
311. Какой тип химической связи характерен для вещества с формулой С3 Н7 ОН?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
312. Какой химической реакцией можно распознать крахмал среди других веществ?
А) реакция «серебряного зеркала», Б) реакцией с сульфатом меди,
В) с раствором йода, Г) реакцией с оксидом меди при нагревании.
313. Сколько граммов воды требуется для приготовления 130 г раствора сахара с массовой долей 20% ? А) 84 Б) 104 В) 114 Г) 94
134. Гидролиз вещества NaNO2 происходит:
А) по катиону, Б) по аниону,
В) и по катиону, и по аниону, Г) гидролиз не идет.
315. Какая реакция идет с большей скоростью?
А) Fe (гранулы) + 5% р-р серной кислоты, Б) Fe (пыль) + 5% р-р серной кислоты,
В) Fe (гранулы) + 10% р-р серной кислоты, Г) Fe (пыль) + 10% р-р серной кислоты
316. Какие соли получаются при взаимодействии избытка кислоты со щелочью?
А) средние, Б) основные, В) кислые, Г) комплексные
317. Как получают алюминий?
А) электролизом хлорида алюминия,
Б) вытеснением из раствора соли более активным металлом,
В) электролизом оксида алюминия в криолите,
Г) восстановлением из оксида с помощью водорода
318. Подберите к левой части уравнения реакции правую: Fe +H2SO4(конц) →
A) → SO2 + H2O + FeSO4 Б) → S + H2O + FeSO4
В) → SO2 + H2O + Fe2 (SO4)3 Г) реакция не идет, железо пассивируется
319. Какова массовая доля глицина в растворе, полученном при смешении 40 г глицина и 1000 г воды? А) 4.0% Б) 25% В) 50% Г) 3.8%
320. Поливинилхлорид и тефлон являются:
А) каучуками, Б) пластмассами, В) волокнами, Г) искусственной кожей
321. Как распознать соли сероводородной кислоты сульфиды среди других веществ?
А) при добавлении раствора щелочи образуется белый осадок, растворяющийся в избытке щелочи,
Б) при добавлении щелочи выпадает бурый осадок,
В) при добавлении лакмуса малиновый цвет,
Г) при добавлении сильной кислоты образуется газ с запахом тухлых яиц
322. К левой части уравнения реакции подберите правую часть: Cu + НС1 →
А) реакция не идет; Б) → CuCl2 + H2; В) → CuCl + H2; Г) → CuClН;
323. Ангидриды органических кислот поучают:
А) отщеплением воды от одной молекулы кислоты, Б) присоединением хлора
В) изомеризацией кислоты, Г) отщеплением воды от двух молекул кислоты
324. Какой химической реакцией можно распознать нерастворимые в воде белки?
А) ксантопротеиновой реакцией, Б) биуретовой реакцией,
В) взаимодействием с ацетатом свинца, в результате черный осадок,
Г) при сгорании запах «жженных перьев»
325. Порядок соединения атомов в молекуле (строение вещества) показывает формула:
А) эмпирическая, Б) молекулярная, В) структурная, Г) сокращенная.
326. Как распознать растворимые соли алюминия среди других веществ?
А) при добавлении раствора щелочи образуется белый осадок, растворяющийся в избытке щелочи,
Б) при добавлении щелочи выпадает бурый осадок,
В) при добавлении лакмуса малиновый цвет,
Г) при добавлении сильной кислоты образуется газ с запахом тухлых яиц
327. Гидроксид бария реагирует с каждым из двух веществ:
А) N2O5, KCl Б) HNO3, ZnCl2 В) KOH , SO2 Г) K2O, H2O
328. Какое из соединений азота в химических реакциях может проявлять только восстановительные свойства?
а) N2 Б) NH3 В)HNO3 Г) NO
329. Высший оксид элемента азота: А) NO Б) NO2 В) NO3 Г) N2 O5
330. Какой тип химической связи характерен для вещества с формулой Н2CO3 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
331. Кто автор теории « Атомы в молекулах соединены друг другом согласно их валентности, причем углерод в органических веществах всегда четырехвалентен»?
А) Менделеев, Б) Берцелиус, В) Бутлеров, Г) Аррениус.
332. Какова степень окисления атома фосфора в веществе с формулой AlPO4 ?
А) +2 Б) -2 B) + 4 Г) +5 Д) +3 Е) - 3.
333. Какой химической реакцией можно распознать вещества с двойными С=С связями ?
А) раствором марганцовки, Б) с водородом, В) с хлором,
Г) реакцией «серебряного зеркала»
334. Какая масса уксусной кислоты содержится в 150 граммах «магазинного» раствора с массовой долей 6% ? А) 12 г Б) 9 г В) 6 г Г) 24 г
325. Гидролиз вещества BaSO4 происходит:
А) по катиону, Б) по аниону, В) и по катиону, и по аниону, Г) гидролиз не идет.
326. В реакции нейтрализации при избытке кислоты и недостатке щелочи образуется соль:
А) средняя, Б) кислая, В) основная, Г) комплексная
327. Как распознать растворимые соли ЖЕЛЕЗА (III) среди других веществ?
А) при добавлении раствора щелочи образуется белый осадок, растворяющийся в избытке щелочи,
Б) при добавлении щелочи выпадает бурый осадок,
В) при добавлении лакмуса малиновый цвет,
Г) при добавлении сильной кислоты образуется газ с запахом тухлых яиц
328. На воздухе в присутствии влаги ржавеет. Выберите схему уравнения этой реакции:
А) Fе + O2 + Н2О → Fе(ОН)2 Б) Fе + O2 + Н2О → Fе(ОН)3
В) Fе + O2 + Н2О → Fе(ОН)4 Г) Fе + O2 + Н2О → Fе(ОН)
329. Как называется химической вещество, имеющее формулу Na2CO3∙ 10H2O?
А) каустическая сода, Б) пищевая сода, В) кристаллическая сода, Г) горькая соль.
340. Выбрать формулу для вычисления массы вещества в растворе:
А)![]() Б)
Б) ![]() В)
В) ![]()
Г) ![]()
341. Какой реакцией можно распознать раствор фенола среди других веществ?
А) выпадением осадка серебра при добавлении аммиачного раствора оксида серебра,
Б) появление фиолетовой окраски при добавлении раствора FeCl3,
В) появлением специфичного запаха при нагревании,
Г) появлением запаха «жженных перьев» при сгорании.
342. Вещества, имеющие одинаковый состав, но различное строение и свойства, называются:
А) изомеры, Б) гомологи, В) окислители, Г) ингибиторы.
343. Как можно сместить химическое равновесие реакции С ТВ + СО2 газ → 2СО газ – Q в правую сторону?
А) +Р, Б) -с (С) В) +с (СО) Г) +t
344. Гидролиз вещества СuCl2 происходит:
А) по катиону, Б) по аниону, В) и по катиону, и по аниону, Г) гидролиз не идет.
345. Как распознать соли карбонаты среди других веществ?
А) при добавлении щелочи образуется синий осадок,
Б) при добавлении нитрата серебра выпадает белый творожистый осадок;
В) при добавлении соляной кислоты выделяется бесцветный газ, от которого мутнеет известковая вода,
Г) при добавлении нитрата серебра выпадает желтый осадок.
346. Определите объем азота, который образуется при полном сгорании этиламина массой 5,13 г. при н.у.
А)2.6 л Б) 12 л В)1.28 л Г) 4.0 л
347. Выберите уравнение реакции алюминотермии:
А) 4Аl + 3МnО2 → 2А12О3 + 3Мn Б) 4Аl + 3О2 → 2А12О3
В) 2Al + 6H2O → 2Al(OH)3 + 3H2 Г) 2Al + N2 –t°→ 2AlN
348. Применяемые в быту металлические предметы (кастрюли) защищены от коррозии с помощью:
А) протектора Б) минерального масла В) ингибитора Г) эмали
349. Вычислить массовую долю вещества в растворе, который получен при смешивании 100 г удобрения и 1 л воды. А) 9% Б) 20% В) 17% Г) 26%
350. Что обозначает порядковый номер элемента?
А) число внешних электронов, Б) валентность,
В) количество электронных слоев, Г) заряд ядра атома.
351. Реакция, в которой все реагенты и продукты жидкости, называется:
А) сложной, Б) гетерогенной, В) экзотермической, Г) гомогенной
352. Даны: раствор яичного белка, раствор муравьиного спирта, гексен-2. Какой химической реакцией можно распознать раствор белка?
А) посинение при добавлении йодной воды желтого цвета, Б) биуретовой реакцией,
В) добавлением активного металла, Г) изменением окраски раствора перманганата калия.
353. Как распознать растворимые соли меди (II) среди других веществ?
А) при добавлении щелочи образуется синий осадок,
Б) при добавлении нитрата серебра выпадает белый творожистый осадок;
В) при добавлении соляной кислоты выделяется бесцветный газ, от которого мутнеет известковая вода,
Г) при добавлении нитрата серебра выпадает желтый осадок.
354. Подберите правую часть для схемы реакции Zn(OH)2 + NaOH (раствор) →
А) → Na2ZnO2 + H2O Б) → NaZnOH + H2
В) → ZnO + NaO + H2O Г) → Na2[Zn(OH)4]
355. В реакциях с неметаллами щелочные металлы являются:
А) окислителями Б) восстановителями
В) в некоторых реакциях - окислителями, в некоторых реакциях - восстановителями,
Г) ни окислительных, ни восстановительных свойств не проявляют
356. Количество внешних электронов в атоме калия равно: А) 4, Б) 3, В) 2, Г) 1.
357. Наиболее ярко выраженные металлические свойства проявляет:
А) галлий, Б) индий; В) алюминий, Г) бор.
358. Высший оксид элемента кремния: А) SiO Б) SiO2 В) SiO3 Г) SiO4
359. Какой тип химической связи характерен для вещества с формулой СО2 ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
360. Кто автор тории «Свойства органических веществ определяются не только их количественным составом, но и порядком связи атомов в молекуле, т.е. химического строения» ?
А) Велер, Б) Авогадро, В) Бутлеров, Г) Менделеев.
361. Элементарные частицы атома зарядом 0 и массой 1 называются:
А) позитроны, Б) протоны, В) нейтроны, Г) электроны
362. Сколько процентов составляет 50 г сахара, растворенный в в 1 л воды? Ответ округлить до десятых. А) 3,2 Б) 4,8 В) 50, Г) 1,2
363. Присоединение водорода к органическому веществу называется:
А) гидрирование, Б) гидратация, В) галогенирование, Г) окисление.
364. Выберите структурные формулы изомера гексана:
А) ![]() Б)
Б) ![]()
В) ![]() Г)
Г) 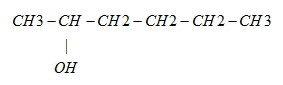
365. Даны: пропиловый спирт, пропионовая кислота, пропионовый альдегид. Какой химической реакцией можно распознать карбоновые кислоты?
А) реакцией «серебряного зеркала»,
Б) при взаимодействии с активными металлами выделяется газ,
В) обесцвечиванием бромной воды, Г) изменением цвета лакмуса
366. Как распознать соли ортофосфорной кислоты среди других веществ?
А) при добавлении щелочи образуется синий осадок,
Б) при добавлении нитрата серебра выпадает белый творожистый осадок;
В) при добавлении соляной кислоты выделяется бесцветный газ, от которого мутнеет известковая вода,
Г) при добавлении нитрата серебра выпадает желтый осадок.
367. Гидроксид алюминия проявляет амфотерные свойства при взаимодействии с
А) NaOH и Cs2SO4 В) H2SO4 и KOH Б) KOH и Na2 O Г) HCl и CaCl2
378. Закончить схему уравнения реакции FeCl3 + KOH→
А) → Fe(OH)2 + KCl Б) → Fe(OH)3 + KCl
В) → Fe(OH) + KClO Г) → KFe + HClO
369. Как распознать соли хлороводородной кислоты среди других веществ?
А) при добавлении щелочи образуется синий осадок,
Б) при добавлении нитрата серебра выпадает белый творожистый осадок;
В) при добавлении соляной кислоты выделяется бесцветный газ, от которого мутнеет известковая вода, Г) при добавлении нитрата серебра выпадает желтый осадок.
370. В реакции Na + O2 → образуется:
А) оксид натрия Б) пероксид натрия, В) гидроксид натрия Г) надпероксид натрия
371. Название наиболее известного сплава на основе алюминия :
А) хромалюминий, Б) магналий, В) дюралюминий, Г) латунь
372. Наиболее ярко выраженные металлические свойства проявляет:
А) кальций, Б) скандий; В) калий, Г) титан.
373. Высший оксид элемента бора: А) В2O Б) В2O2 В) В2O3 Г) В2O5.
374. Отрицательно заряженный ион называется: А) катод Б) анод В) катионы Г) анионы.
375. Какова степень окисления атома меди в веществе с формулой Сu2O:
А) +2 Б) -2 B) 0 Г) -1 Д) +1 Е) - 3.
376. Какой тип химической связи характерен для вещества с формулой СН3СООН ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
377. Порошок белого цвета, не растворимый в холодной и набухающий в горячей воде с образованием клейстера: А) глюкоза, Б) крахмал, В) целлюлоза, Г) фруктоза.
378. При омылении этилацетата получили этанол массой 20.7 г. Определите массу сложного эфира, который вступил в реакцию. А) 12.4 г Б)10,35 г В)42, 1 г Г) 39.6 г
379. Основным типом реакции для алкенов и веществ с добавочной связью является:
А) замещение, Б) присоединение, В) разложение, Г) изомеризация.
380. Этан и гексан являются:
А) гомологами, Б) изомерами, В) полимерами, Г) жидкостями.
381. Как распознать азотную кислоту и ее соли среди других веществ?
А) при добавлении к ним концентрированной серной кислоты и меди выделяется бурый газ;
Б) при добавлении к ним раствора гидроксида калия выпадет синий осадок;
В) при добавлении к ним лакмуса окраска изменится на синий,
Г) при добавлении к ним магния или цинка выделится бесцветный газ.
382. Оксид натрия реагирует с каждым из двух веществ:
А) Cu(NO3)2 , K2SO4 Б) CO2, H2SO4 В) Al(OH)3, CuCl2 Г) CO2 , KNO3
383. Закончите уравнение реакции: S + HNO3(конц) →
А) → H2S + NO3 + H2 Б) → H2SO4 + NO2 + H2O
В) →H2SO3 + NO + H2O Г) → SO3 + NO + H2O
384. Наиболее ярко выраженные металлические свойства проявляет:
А) натрий, Б) магний; В) кремний, Г) алюминий.
385. Высший оксид элемента бария: А) Ва2O Б) Ва2O4 В) Ва2O3 Г) ВаO.
386. Положительно заряженный электрод при электролизе называется
А) катод Б) анод В) катионы Г)анионы.
387. Какой тип химической связи характерен для вещества алюминия ?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
388. Какова степень окисления атома серы в веществе с формулой BaSO4?
А) +2 Б) + 7, B) + 4 Г) +6 Д) +3 Е) - 3.
389. Сколько граммов соли содержится в 120 граммах раствора с массовой долей 20 % ?
А) 12 Б) 24, B) 20 Г) 100
390. Белое волокнистое вещество, не растворимое в воде, в кислотах и органических растворителях:
А) глюкоза, Б) крахмал, В) целлюлоза, Г) фруктоза.
391. Вещества СН3-СН2-ОН и СН3-О- СН3 являются:
А) гомологами, Б) изомерами, В) кислотами, Г) полимерами.
392.При изменении температуры на каждые 10 градусов скорость реакции изменяется в:
А) 2-10 раз, Б) 2-4 раза, В) 5 раз, Г) 2-5 раз
393. Какие продукты образуются при взаимодействии фтора с водой:
А) = HF + H2O Б) =HF + O2 В) = HF + H2 Г) = CaF2 + H2
394. Закончите уравнение реакции: H3PO4 + 2NaOH →
А) → NaH2PO4 + H2O Б) → Na2HPO4 + 2H2O
В) → Na3HPO4 + 2H2O Г) → Na3PO4 + 2H2O
395. Основным сырьем первой стадии получения азотной кислоты являются:
А) азот и кислород, Б) аммиак и кислород, В) водород и кислород,
Г) оксид азота (II) и кислород
396. Эластичные полимеры: А) пластмассы, Б) каучуки, В) волокна, Г) крахмал
397. Нельзя практически осуществить реакцию:
А) КI + Cl2 = Б) KI + Br2 = B) KBr + Cl2 = Г) KCl + Br2 =
398. Вещество с химической формулой СО является:
А) кислотным оксидом, Б) амфотерным оксидом,
В) несолеобразующим оксидом, Г) основным оксидом
399. Сплав железа с углеродом (массовая доля углерода 2- 4%), с малым количеством серы, фосфора, марганца и др. металлов называется: А) латунь, Б) бронза, В) чугун, Г) сталь
400. Закончите уравнение реакции: Ca3(PO4)2 + C + SiO2 →
А) → СаС2 + CO2 + SiO2 Б) → P + CO2 + CaSi
В) → P2О5 + C + CaSiO3 Г) → P + CO + CaSiO3
401. Химическое равновесие в системе 2NO(г) + O2 (г) → 2NO2 (г) + Q смещается в сторону образования продукта реакции при:
А) повышении давления, Б) повышении температуры,
В) понижении давления, Г) применении катализатора
402. Укажите обратимую реакцию. А) 2Al + 3O2 = Al2O3
Б) 2Na + 2H2O = 2NaOH + H2 В) N2 + 3H2 = 2NH3 Г) C3H8 + 5O2 = 3CO2 + 4H2O
403. Способность атома химического элемента оттягивать на себя общую электронную пару химической связи (или отнимать электроны от атома другого вида):
А) электроотрицательность, Б) радиус, В) валентность, Г) растворимость.
404. Сколько литров аммиака выделится при взаимодействии 67.2 литров водорода с избытком азота (при 100%-ном выходе аммиака)? А) 22.4 л, Б) 44.8 л, В) 67,2 л, Г) 112 л.
405. Чем лучше скрепить две цинковые пластинки, чтобы их коррозия не ускорилась:
А) медной проволокой, Б) железной проволокой, В) алюминиевой проволокой.
406. Наиболее ярко выраженные неметаллические свойства проявляет:
А) бром, Б) астат; В) иод, Г) хлор.
407. Высший оксид элемента натрия: А) Na2O Б) Na2O2 В) Na2O5 Г) NaО3
408. Выберите ряд, включающий только оксиды:
А) СuO , BaO, СаO, Б) SO2 H2S, H2O B) H2O, PH3, SO3 Г) HI, H3PO4, HClO
409. Какой тип химической связи характерен для вещества с формулой HF?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
410. Кто автор закона о том, что в одинаковых объемах разных газов содержится одинаковое число молекул?
А) Менделеев, Б) Бутлеров, В) Аррениус, Г) Авогадро.
411. Общая формула алканов: А) СnH2n+2 Б) ) СnH2n-4 В) СnH2n-2 Г) СnH2n
412. Названия алкинов заканчиваются на : А) –ен, Б) –ол, В) -аль, Г) –ин.
413. При расщеплении крахмала образуется: А) глюкоза, Б) фруктоза, В) сахароза, Г) рибоза
414. Какая из реакций является окислительно-восстановительной, допишите ее:
А) Fe + HCl →, Б) МgO + HCl →, В) Mg(OH)2 + HCl → Г) MgSO4 + BaCl2 →
415. В пронумерованных пробирках без названий два раствора: силиката натрия и карбоната калия. Как распознать эти вещества?
А) добавлением сильной кислоты, Б) с помощью лакмуса,
В) добавлением цинка, Г) добавлением глицерина
416. Подберите правильный результат для реакции: P2O5 + H2O (горячая) =
А) = HPO3 Б) = HPO В) = H4 P2 O7 Г) = H3 PO4
417. Как получают в промышленных масштабах кислород?
А) электролизом воды, Б) разложением перманганата калия,
В) выделение из сжиженного воздуха, Г) разложением серной кислоты
418. Каким способом получают в промышленности железо (сталь)?
А) пирометаллургией; Б) электролизом различных солей;
В) гидрометаллургией Г) металлотермией.
419. Написать уравнения реакций по схеме
CH3COOH → CH2 (Cl)COOH → CH2 (OH)COOH → CH2 (OH)COOK
420.Какой объем кислорода и углекислого газа содержится в 500 м3 воздуха? (Объемная доля кислорода в воздухе – 21%, углекислого газа – 0,04%)
А) 105; 0,20, Б) 10,5; 2, В) 200; 40, Г) 150; 30.
421. Величина, равная отношению массы вещества к массе раствора, выраженная в % называется:
А) масса, Б) массовая доля, В) концентрация, Г) количество вещества.
422. Химическая связь, возникающая между катионами металлов и анионами неметаллов за счет их электростатического притяжения:
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
423. Вычислите объем водорода, который образуется при растворении алюминия массой 8,1 г в воде.
А) 3,6 Б) 6,7 В) 5 Г) 10
424. Количество электронов в атоме брома равно: А) 40, Б) 35, В) 80, Г) 45.
425. Наиболее ярко выраженные металлические свойства проявляет:
А) бор, Б) углерод; В) бериллий, Г) литий.
426. Высший оксид элемента кальция: А) Са2O Б) Са2O2 В) Са2O5 Г) СаО
427. Выберите ряд, включающий только оксиды:
А) СuO , BaO, Са(OН)2, Б) SO2 , HNO3, Cl2O, B) H2O, PH3, SO3 Г) CO, ZnO, ClO
428. Частица Ва2+ называется :
А) электрон бария Б) атом бария В) катион бария Г) анион бария.
429. Железо относится к семейству элементов:
А) s-элементам Б) p-элементам, В) d-элементам Г) f-элементам.
430. Какова массовая доля кислоты в растворе, полученном при смешении 10 г серной кислоты и 50 г воды? Ответ округли до целого числа А) 10% Б) 20 % В) 15% Г) 17%
431. Расставьте коэффициенты в уравнениях: Аl+ Н2SO4 → Al2(SO4)3 + H2 ;
Чему равен коэффициент перед восстановителем в этом уравнении?
А) 2, Б) 3, В) 4 Г) 6
432. Растительные жиры жидкие, потому что содержат:
А) остатки непредельных кислот, Б) глицерин, В) атомы натрия,
Г) растительные масла тают из-за высокой температуры.
433. Эластичные полимеры: А) пластмассы, Б) каучуки, В) волокна, Г) крахмал
434. Нельзя практически осуществить реакцию:
А) КI + Cl2 = Б) KI + Br2 = B) KBr + Cl2 = Г) KCl + Br2 =
435. Вещество с химической формулой СО является: А) кислотным оксидом,
Б) амфотерным оксидом, В) несолеобразующим оксидом, Г) основным оксидом
436. Сплав железа с углеродом (массовая доля углерода 2- 4%), с малым количеством серы, фосфора, марганца и др. металлов называется:
А) латунь, Б) бронза, В) чугун, Г) сталь
437.Углеводороды, в молекулах которых содержится одна тройная С ≡ С связь:
А) карбоновые кислоты, Б) алкены, В) алкины, Г) амины.
438. Общая формула альдегидов: А) R-CnH2n Б) R-CnH2n+2 В) R-CHO Г) CnH2n+1OH
439. Выбрать реакцию гидрирования:
А) CH2=CH2 + HOH → CH3-CH2-OH, Б) CH2=CH2 + HBr → CH3-CH2-Br,
В) CH2=CH2 + H2 → CH3-CH3, Г) CH2=CH2 + Br2 -→ Br-CH2-CH2-Br,
440. Вещества, сходные по строению и свойствам, но отличающиеся друг от друга по составу на одну или несколько групп –СН2-: А) спирты, Б) гомологи, В) углеводороды, Г) белки.
441. Как называется вещество с формулой CH3- CH2-СН2-ОН:
А) пропанол, Б) пропаналь, В) пропановая кислота, Г) пропанон.
442. Написать уравнения реакций по схеме: CH4 → C2H2 → С6Н6 → С6Н5-Cl
443. Выбрать фактор, который смещает химическое равновесие реакции I2 + H2 → 2HI + Q в сторону образования продуктов реакции: А) +Р, Б) –t, В) +t, Г) +с(HI).
444. Величина, равная отношению массы вещества к молярной массе этого же вещества, называется:
А) масса, Б) объем, В) концентрация, Г) количество вещества.
445. Химическая связь, возникающая между атомами неметаллов за счет образования общих электронных пар: А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
446. При электролизе расплава хлорида натрия был получен натрий массой 4,6 г. Рассчитайте массу хлора, который образовался. А) 42 Б) 46 В) 10 Г) 7.1
447. Число протонов в атоме натрия равно: А) 11, Б) 23, В) 12, Г) 3.
448. Наиболее ярко выраженные неметаллические свойства проявляет:
А) бор; Б) азот; В) углерод, Г) фтор.
449. Высший оксид элемента брома: А) Br2O Б) Br2O7 В) Br2O5 Г) BrО3
450. Выберите группу, включающую только сложные вещества:
А) SO2 , BaO, Са Б) O2, N2, Fe, CO B) H2O, PH3, SO3 Г) Ba, P2O5, Cl2, C
451. Элементы главных подгрупп 3-8 групп относятся к элементам:
А) s-семейства, Б) р-семейства, В) d-семейства, Г) f-семейства.
452. Какой тип химической связи характерен для вещества с формулой O2?
А) ковалентная, Б) ионная, В) металлическая, Г) водородная.
453. Требуется получить стекло состава Na2O*CaO*6SiO2 массой 10 кг. Рассчитайте массу соды Na2CO3 в килограммах, который потребуется для получения этого стекла.
А) 7.5 Б) 13 В) 5.2 Г) 3.9
454. Названия алкенов заканчиваются на : А) –ен, Б) –ол, В) -аль, Г) –ин.
455. Гидролиз вещества Na CH3COO происходит:
А) по катиону, Б) по аниону, В) и по катиону, и по аниону, Г) гидролиз не идет.
456. Выберите дисахарид: А) (С6Н10О5)n Б) С6Н12 О6 В) С12Н22О11 Г) С10Н22
457. В пронумерованных пробирках без названий 2 вещества: азотная кислота и гидроксид калия. Как распознать эти вещества?
А) добавлением концентрированной серной кислоты и меди, Б) с помощью лакмуса,
В) нагреванием, Г) добавлением этилового спирта
458. Подберите правильный результат для реакции: NH4NO3 + Ca(OH)2 =
А) = Ca(NO3)2 + NH3 + H2O Б) = CaNH4 + NO3OH
В) = Ca + NH4 + NO2 + H2O Г) = Ca(NO3)2 + H2O
459. Каким способом получают в промышленности металлический натрий?
А) разложением гидроксида натрия;
Б) электролизом расплава поваренной соли;
В) окислением сульфата натрия
Г) взаимодействием поваренной соли с бромом.
 Получите свидетельство
Получите свидетельство Вход
Вход












 Примерные тестовые задания для подготовки к дифференцированному зачету по химии (250.51 KB)
Примерные тестовые задания для подготовки к дифференцированному зачету по химии (250.51 KB)
 0
0 136
136 1
1 Нравится
0
Нравится
0


